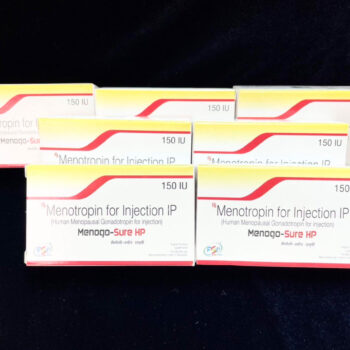
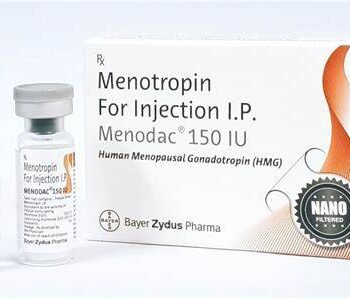
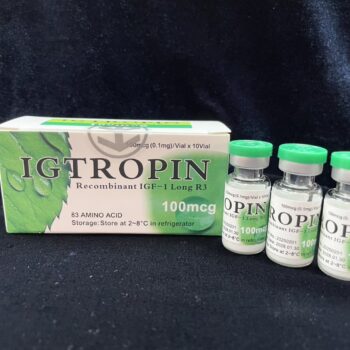
** 日本へのお客様 **
税関で注射剤と判明した場合、2020年からは薬物監視の証明の提示が求められます。
薬物監視証明が用意できない場合は、手続きに従い送り主に返送してください。
商品が弊社に到着しましたらご連絡させていただきますので、再度送料をお支払いいただいた上で再発送させていただきます。
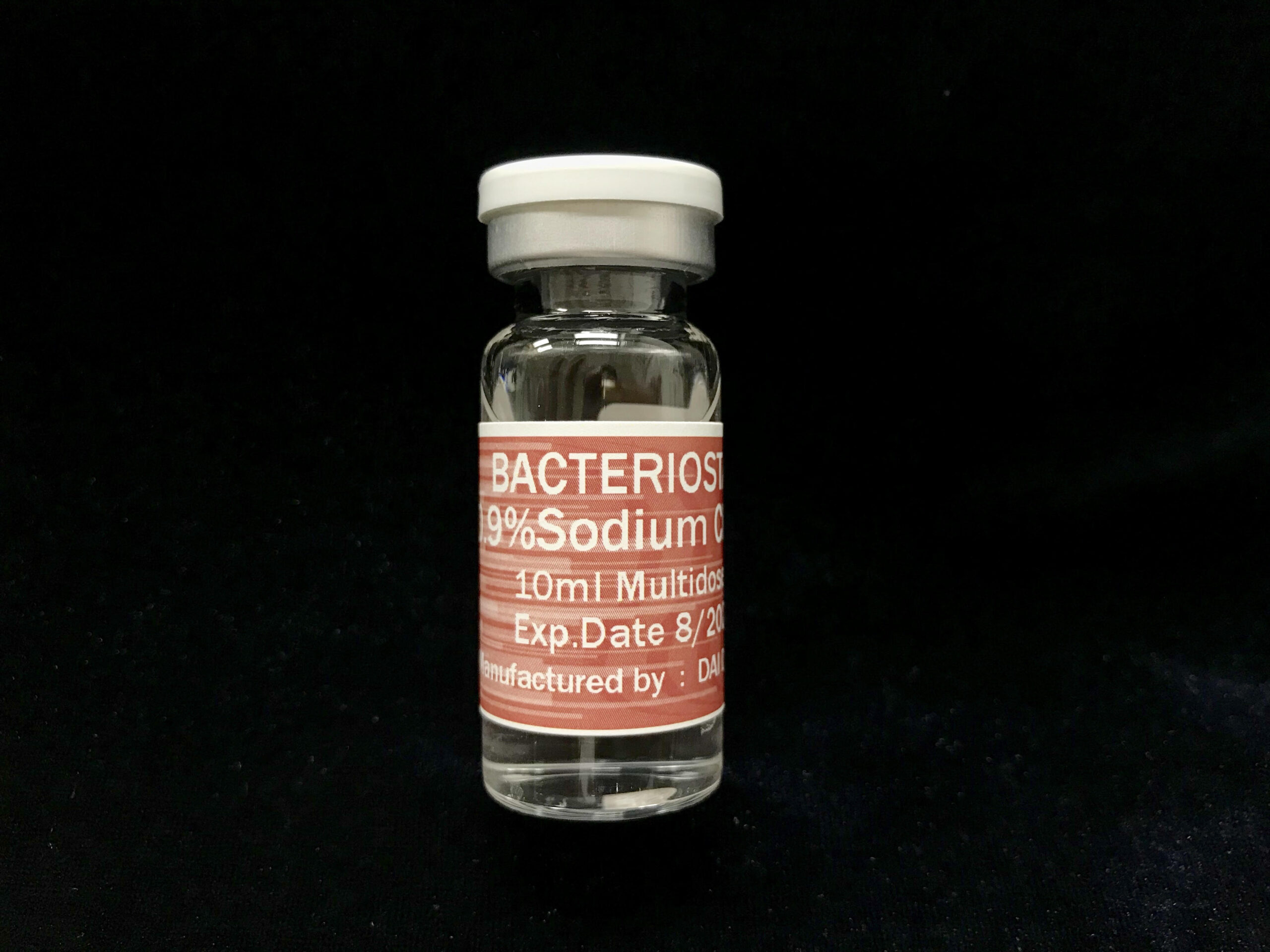
殺菌剤 0.9%塩化ナトリウム 10cc/バイアル
説明
この製剤は、注射前に希釈を必要とする薬剤、または水性媒体に溶解する必要がある薬剤を追加した後にのみ、非経口投与するように設計されています。
殺菌性 0.9% 塩化ナトリウム注射液 USP は、注射用水に溶解した滅菌済み、非発熱性、塩化ナトリウムの等張液です。1 ミリリットル (mL) あたり、殺菌性防腐剤として塩化ナトリウム 9 mg とベンジルアルコール 0.9% (9 mg/mL) が含まれています。pH 調整用に塩酸が含まれている場合があります。複数回投与容器で供給され、繰り返し取り出して投薬用に薬剤を希釈または溶解することができます。pH は 5.0 (4.5 ~ 7.0) です。
塩化ナトリウム (USP) は化学的には NaCl と指定され、水に自由に溶ける白い結晶性粉末です。
半硬質バイアルは、特別に配合されたポリオレフィンから製造されています。これはエチレンとプロピレンの共重合体です。プラスチックの安全性は、プラスチック容器に関する USP 生物学的基準に従って動物実験で確認されています。適切な薬物濃度を維持するために容器に蒸気バリアは必要ありません。
臨床薬理学
水中の塩化ナトリウムは解離してナトリウムイオン(Na+)と塩化物イオン(Cl−)を生成します。これらのイオンは体液(主に細胞外)の正常な成分であり、電解質バランスを維持するために不可欠です。
ナトリウム(Na+)と塩素(Cl−)の分布と排泄は主に腎臓によって制御されており、腎臓は摂取量と排出量のバランスを維持しています。
細菌静止剤 0.9% 塩化ナトリウム注射液 (USP) によって提供される少量の液体と少量の塩化ナトリウムは、薬剤の非経口注射の媒体としてのみ使用される場合、新生児や非常に小さい乳児を除いて、体液と電解質のバランスに大きな影響を与える可能性は低いと考えられます。
水はすべての体組織の必須成分であり、体重の約 70% を占めます。成人の 1 日の平均的な必要量は 2 ~ 3 リットルです (発汗と尿の生成による不感水分損失はそれぞれ 1.0 ~ 1.5 リットル)。
水分バランスは、さまざまな調節機構によって維持されます。水分の分配は主に体の各部における電解質の濃度に依存し、ナトリウム (Na+) は生理的平衡の維持に大きな役割を果たします。
適応症と使用法
この非経口製剤は、投与する薬剤の製造元の指示に従って、静脈内、筋肉内または皮下注射用に薬剤を希釈または溶解するためにのみ適応されます。
CONTRAINDICATIONS
Due to the potential toxicity of benzyl alcohol in neonates, solutions containing benzyl alcohol must not be used in this patient population.
Parenteral preparations with benzyl alcohol should not be used for fluid or sodium chloride replacement.
Parenteral preparations containing benzyl alcohol should not be used in epidural or spinal anesthetic procedures.
WARNINGS
Benzyl alcohol, a preservative in Bacteriostatic Sodium Chloride Injection, USP has been associated with toxicity in neonates. Data are unavailable on the toxicity of other preservatives in this age group. Preservative-free Sodium Chloride Injection should be used for flushing intravascular catheters. Where a sodium chloride solution is required for preparing or diluting medications for use in neonates, only preservative-free Sodium Chloride Injection should be used.
PRECAUTIONS
Consult the manufacturer’s instructions for choice of vehicle, appropriate dilution or volume for dissolving the drugs to be injected, including the route and rate of injection.
Inspect reconstituted (diluted or dissolved) drugs for clarity (if soluble) and freedom from unexpected precipitation or discoloration prior to administration.
Pregnancy
Animal reproduction studies have not been conducted with Bacteriostatic 0.9% Sodium Chloride Injection, USP. It is also not known whether Bacteriostatic 0.9% Sodium Chloride Injection containing additives can cause fetal harm when administered to a pregnant woman or can affect reproduction capacity. Bacteriostatic 0.9% Sodium Chloride Injection containing additives should be given to a pregnant woman only if clearly needed.
Pediatric Use
The safety and effectiveness in the pediatric population are based on the similarity of the clinical conditions of the pediatric and adult populations. However, due to potential toxicity of benzyl alcohol in neonates, solutions containing benzyl alcohol are contraindicated in this patient population.
Drug Interactions
Some drugs for injection may be incompatible in a given vehicle, or when combined in the same vehicle or in a vehicle containing benzyl alcohol. Consult with pharmacist, if available.
Use aseptic technique for single or multiple entry and withdrawal from all containers.
When diluting or dissolving drugs, mix thoroughly and use promptly.
Do not store reconstituted solutions of drugs for injection unless otherwise directed by the manufacturer of the solute.
Do not use unless the solution is clear and seal intact.
ADVERSE REACTIONS
Reactions which may occur because of this solution, added drugs or the technique of reconstitution or administration include febrile response, local tenderness, abscess, tissue necrosis or infection at the site of injection, venous thrombosis or phlebitis extending from the site of injection and extravasation.
有害反応が起こった場合は、点滴を中止し、患者を評価し、適切な対策を講じ、可能であれば、未使用の溶媒の残りを回収して検査のために保存してください。
0.9% ベンジルアルコールの静脈内、筋肉内、または皮下注射によるヒトへの有害反応は知られていないが、数種の動物における 0.9% ベンジルアルコールを含む少量の非経口製剤の実験的研究により、成人に最大 30 mL の静脈内投与を毒性作用なしに安全に投与できることが示された。6 kg の新生児または乳児に推定 9 mL を投与すると、血圧の変化を引き起こす可能性がある。